安徽生物制品宿主細胞殘留DNA檢測
來源:
發布時間:2025-08-13
湖州申科生物rHCDpurify® 前處理系統是用于宿主細胞殘留 DNA 檢測樣本前處理的得力工具,具備諸多優勢。在操作便捷性上,它支持自動掃碼,輸入準確且簡單高效,同時配備超大視屏,方便操作人員使用。溫控方面表現出色,能精確控溫,這有助于提高裂解和洗脫效率,減少因溫度控制不當帶來的系統誤差,為后續檢測奠定良好基礎。從提取性能來看,該系統符合系統性能驗證和挑戰性實驗要求,能夠可靠地完成樣本前處理工作,保障檢測的準確性與可靠性。在試劑配套上,它搭配 SHENTEK® 各類前處理試劑盒,可有效避免手動操作產生的誤差,確保實驗結果的穩定性。此外,該系統具備多種程序模式,能實現磁珠法試劑盒和樣本前處理的自動化提取操作,不僅提高了工作效率,還減少了人工干預可能帶來的誤差,為宿主細胞殘留 DNA 檢測樣本前處理提供了穩定、高效、準確的解決方案。
生物制品宿主細胞殘留 DNA 可能存在污染風險,將對產品使用者帶來??潛在安全性影響。安徽生物制品宿主細胞殘留DNA檢測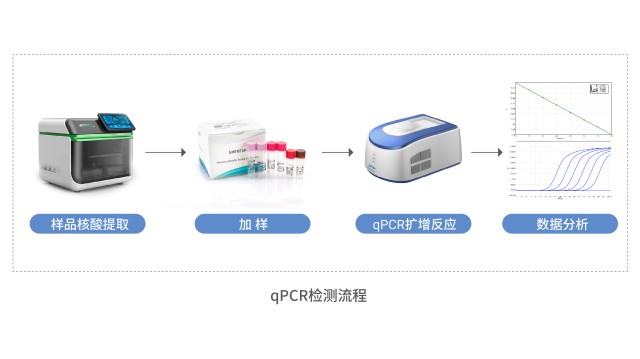
SHENTEK®宿主細胞殘留DNA檢測試劑盒采用抗干擾熱啟動酶和預混型反應體系,簡單高效,耐受干擾;同時采用 dUTP/UNG 防污染系統,性能可靠,特異性強,靈敏度高,定量限可以達到 fg 水平。試劑盒已通過完整的性能驗證,包括線性范圍、準確度、精密度、定量限和專屬性等,性能要求符合藥典標準。還可選購內部陽性質控 IPC(報告基團 VIC)配合使用。產品按照 ISO13485 體系標準化生產,可提供性能驗證報告,已成功用于國內外藥品注冊申報。
山東生物制品宿主細胞殘留DNA檢測生產企業不同類型生物制品對宿主細胞殘留 DNA 檢測樣品處理要求不同。
SHENTEK® E.coli 殘留 DNA 檢測試劑盒是用于定量檢測各種生物制品的中間品、半成品和成品中 E.coli 宿主細胞 DNA 的試劑盒。本試劑盒利用熒光探針原理,定量檢測樣品中 E.coli 殘留 DNA。檢測快速,專一性強,性能穩定可靠,檢測限可以達到 fg 水平。試劑盒配套有E.coli DNA 定量參考品,已嚴格溯源至國家標準品,確保檢測結果的準確性和可追溯性。本試劑盒與SHENTEK宿主細胞殘留 DNA 樣本前處理試劑盒配套使用,可準確定量樣品中 E.coli 殘留 DNA。
美國食品藥品監督管理局(FDA)提醒使用HEK293T細胞生產病毒載體時因存在SV40 T抗原,還需要檢測殘留的腺病毒E1(E1A & E1B)和SV40 T抗原序列。《中國藥典》有關生物制品宿主殘留核酸質量控制要求和CDE頒布的《細胞***產品申請臨床試驗藥學研究和申報資料的考慮要點》中關于質粒和病毒載體的質量標準也提到,如使用HEK293細胞進行病毒載體生產,需進行宿主細胞殘留DNA檢測和RNA殘留、SV40大T抗原DNA殘留、E1A和E1B基因DNA殘留檢測。
宿主細胞殘留DNA檢測是生物制品安全性控制的關鍵指標。
生物制品宿主細胞殘留DNA檢測是生物制藥領域至關重要的質量控制環節,旨在定量監測生物制品(如疫苗、單抗、基因治療產品等)中來源于宿主細胞的DNA殘留量,以評估潛在的安全性風險并確保符合法規要求。其關鍵意義在于:殘留DNA可能攜帶致病基因、病毒序列或致瘤性片段,若未有效控制,可能通過基因整合或免疫原性反應對受者造成風險。基于高靈敏度方法(如定量PCR、雜交法)的宿主細胞殘留DNA檢測并非簡單的合規流程,而是阻斷藥品轉化性風險的科學屏障,是確保每一劑生物藥都能安全惠及患者的必須履行的責任與承諾。湖州申科采用 qPCR 熒光探針法定量檢測各種宿主細胞殘留 DNA,覆蓋常用的生產用工程細胞和載體。江蘇Vero宿主細胞殘留DNA檢測生產企業
SHENTEK? 系列宿主細胞殘留DNA檢測試劑盒適配SHENTEK-96S等常用PCR設備。安徽生物制品宿主細胞殘留DNA檢測
湖州申科生物宿主細胞殘留 DNA 檢測技術服務包括樣品適用性驗證服務,針對樣品做適用性驗證,搭配試劑盒全面性能驗證報告,含精密度(重復性、中間精密度 )、樣品回收率(準確性)驗證,保障檢測結果準確可信 ;提供定制化 HCD 分析方法全面性能驗證服務,對客戶樣品開展線性范圍、準確性等驗證,符合藥典要求并出完整報告 ;此外還有樣品檢測服務,磁珠法自動化提取滿足高通量與提取效率,可檢測多種細胞及病毒殘留DNA,提供 DNA 殘留量與回收率數據 。
安徽生物制品宿主細胞殘留DNA檢測
相關新聞
- 廣東MDCK宿主細胞蛋白(HCP)殘留檢測 2025-08-19
- 浙江E.coli表達菌宿主細胞蛋白(HCP)殘留檢測供應廠家 2025-08-19
- 江蘇單抗藥物用宿主細胞蛋白(HCP)殘留檢測方法開發 2025-08-18
- 成都生物制品宿主細胞蛋白(HCP)殘留檢測試劑盒開發要求 2025-08-18
- 浙江ELISA法宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-08-18
- 釀酒酵母宿主細胞蛋白(HCP)殘留檢測橋接驗證 2025-08-18
- 江蘇工藝特異型宿主細胞蛋白(HCP)殘留檢測常見問題分析 2025-08-18
- 上海單抗藥物用宿主細胞蛋白(HCP)殘留檢測 2025-08-18
- 上海生物制品宿主細胞蛋白(HCP)殘留檢測高風險蛋白 2025-08-18
- 北京BHK宿主細胞蛋白(HCP)殘留檢測常見問題分析 2025-08-18
推薦新聞
- 長寧區什么是醫療管理服務客服電話 2025-08-19
- 天津大鼠ELISA抗體試劑怎么樣 2025-08-19
- 西安新款活性益生菌排名 2025-08-19
- 江蘇脊柱側彎支具一體化 2025-08-19
- Serva膠原酶和胰酶的區別 2025-08-19
- 山東電池模組制造 2025-08-19
- 貴州易清洗的離心振動干燥機電話多少 2025-08-19
- 哪里有平衡測試系統廠家 2025-08-19
- 龍華區標準生物試劑收費 2025-08-19
- 重慶智慧農業葉綠素熒光成像系統 2025-08-19